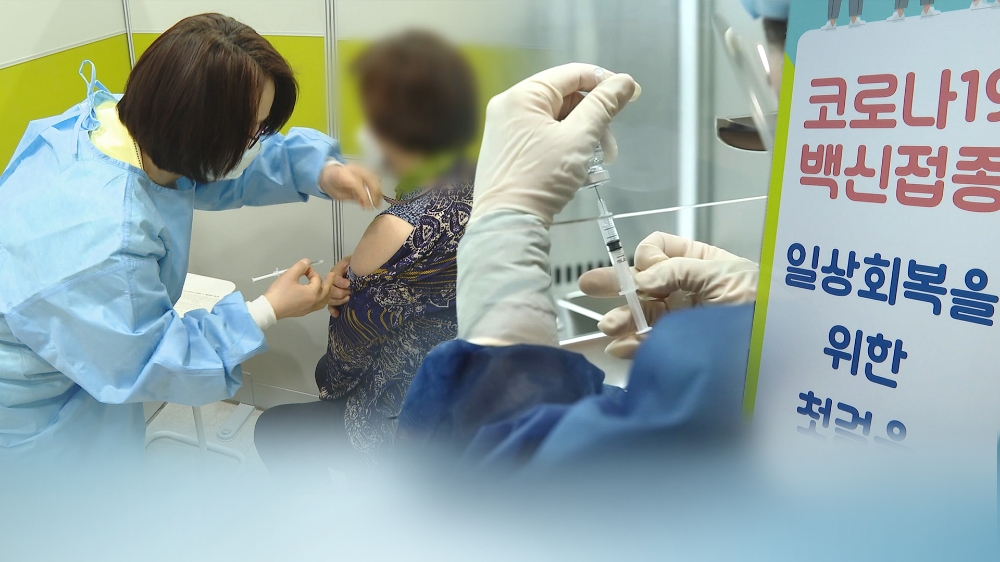
[로이슈 안재민 기자] 백신 등 감염병에 대응하기 위한 의약품 수입 절차가 간소화된다.
식품의약품안전처는 의약품의 신속한 허가와 공급을 위해 이같은 내용을 담아 '생물학적제제 등의 품목허가·심사 규정'을 개정·시행했다고 5일 밝혔다.
개정안에 따라 식약처는 코로나19 백신 등 생물학적 제제를 수입할 때 수출국 정부가 발행한 증명서 제출을 면제하고 해외 규제당국의 허가 여부와 별도로 평가할 예정이다.
동등생물의약품 대조약은 공고된 의약품만 사용할 수 있었으나 식약처는 앞으로 제약사가 신약 및 신약에 준하는 의약품으로 선정할 수 있도록 기준을 제시했다.
또 대체의약품이 없거나 임상시험 대상 환자 수가 극히 적은 경우 임상 3상 시험을 임상 2상 시험 자료로 갈음해 평가할 수 있는 법적 근거를 마련했다.
이를 통해 희귀·난치질환 치료제 허가의 어려움을 해소해 환자 치료기회를 확대할 방침이다.
사용상 주의사항은 국제조화된 기준에 맞춰 사용하도록 하고 신약 품목허가 신청 후 민원인이 담당 부서에 설명회의를 요청할 수 있도록 했다.
안재민 로이슈 기자 newsahn@hanmail.net
식약처, 백신 수입 절차 간소화
기사입력:2021-04-05 10:02:59
<저작권자 © 로이슈, 무단 전재 및 재배포 금지>
로이슈가 제공하는 콘텐츠에 대해 독자는 친근하게 접근할 권리와 정정ㆍ반론ㆍ추후 보도를 청구 할 권리가 있습니다.
메일:law@lawissue.co.kr / 전화번호:02-6925-0217
메일:law@lawissue.co.kr / 전화번호:02-6925-0217
주요뉴스
핫포커스
투데이 이슈
투데이 판결 〉
베스트클릭 〉
주식시황 〉
| 항목 | 현재가 | 전일대비 |
|---|---|---|
| 코스피 | 5,640.48 | ▲90.63 |
| 코스닥 | 1,136.94 | ▼1.35 |
| 코스피200 | 840.89 | ▲14.06 |
가상화폐 시세 〉
| 암호화폐 | 현재가 | 기준대비 |
|---|---|---|
| 비트코인 | 109,994,000 | ▲18,000 |
| 비트코인캐시 | 700,500 | ▼2,000 |
| 이더리움 | 3,431,000 | ▼18,000 |
| 이더리움클래식 | 13,110 | ▲10 |
| 리플 | 2,265 | ▲3 |
| 퀀텀 | 1,403 | ▼8 |
| 암호화폐 | 현재가 | 기준대비 |
|---|---|---|
| 비트코인 | 110,118,000 | ▲63,000 |
| 이더리움 | 3,433,000 | ▼17,000 |
| 이더리움클래식 | 13,070 | ▼30 |
| 메탈 | 438 | ▲1 |
| 리스크 | 207 | ▲1 |
| 리플 | 2,265 | ▲2 |
| 에이다 | 427 | ▼1 |
| 스팀 | 103 | ▼1 |
| 암호화폐 | 현재가 | 기준대비 |
|---|---|---|
| 비트코인 | 110,010,000 | ▼20,000 |
| 비트코인캐시 | 701,500 | ▲1,000 |
| 이더리움 | 3,429,000 | ▼19,000 |
| 이더리움클래식 | 13,070 | ▼30 |
| 리플 | 2,266 | ▲1 |
| 퀀텀 | 1,409 | 0 |
| 이오타 | 98 | 0 |