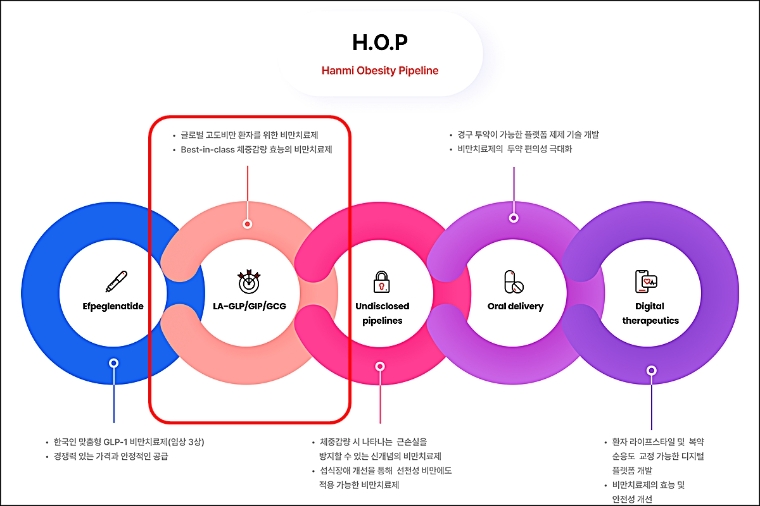
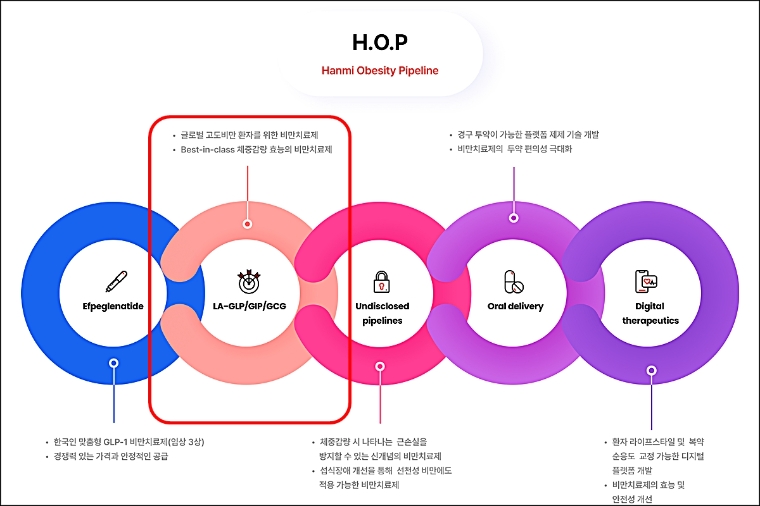
[로이슈 전여송 기자] 한미약품이 지난달 29일(미국 현지시각) 미국 식품의약국(FDA)에 차세대 비만 치료 삼중작용제(LA-GLP/GIP/GCG, 코드명 HM15275)의 임상 1상 진입을 위한 임상시험계획(IND)을 신청했다고 1일 밝혔다.
이는 성인 건강인 및 비만 환자를 대상으로 HM15275의 안전성과 내약성, 약동학, 약력학 특성 등을 평가하는 내용의 임상시험계획이다. 한미약품은 HM15275의 상용화 목표 시점을 2030년으로 설정하고, 지난 2월 29일에는 한국 식품의약품안전처에 IND를 제출하는 등 임상 개발을 속도감 있게 추진해 나가고 있다.
HM15275는 현재 임상 3상 개발이 진행 중인 에페글레나타이드의 혁신을 이어나갈 차세대 비만 신약으로, 글루카곤 유사 펩타이드(GLP-1)와 위 억제 펩타이드(GIP), 글루카곤(GCG) 등 각각의 수용체 작용을 최적화해 ‘근 손실을 최소화하면서도 25% 이상 체중 감량 효과’가 기대되고 있다.
한미약품은 오는 6월 미국에서 열리는 2024 미국당뇨병학회(ADA)에서 HM15275에 대한 여러 건의 주요 연구 결과를 발표할 예정이다. 이번 학회에서 한미약품은 비만 모델에서 체중감량 효능에 대한 HM15275의 계열 내 최고신약 잠재력 및 그 작용 기전을 규명한 결과를 공개한다.
한미약품 최인영 R&D센터장은 “오랜 기간 동안 대사성 질환 분야에서 쌓아온 R&D 역량을 토대로 전 세계적 사회 문제로 대두되고 있는 ‘비만’ 영역에서 새로운 혁신 가능성을 지속적으로 창출해 나가고 있다”며 “제약강국을 향한 열정과 집념으로 가득 찬 한미의 R&D 혁신은 결코 멈추지 않을 것”이라고 강조했다.
전여송 로이슈(lawissue) 기자 arrive71@lawissue.co.kr
한미약품, 美 FDA에 차세대 비만 치료 삼중작용제 임상 1상 IND 신청
기사입력:2024-04-01 16:00:05
<저작권자 © 로이슈, 무단 전재 및 재배포 금지>
로이슈가 제공하는 콘텐츠에 대해 독자는 친근하게 접근할 권리와 정정ㆍ반론ㆍ추후 보도를 청구 할 권리가 있습니다.
메일:law@lawissue.co.kr / 전화번호:02-6925-0217
메일:law@lawissue.co.kr / 전화번호:02-6925-0217
주요뉴스
핫포커스
투데이 이슈
투데이 판결 〉
베스트클릭 〉
주식시황 〉
| 항목 | 현재가 | 전일대비 |
|---|---|---|
| 코스피 | 6,244.13 | ▼63.14 |
| 코스닥 | 1,192.78 | ▲4.63 |
| 코스피200 | 933.34 | ▼10.68 |
가상화폐 시세 〉
| 암호화폐 | 현재가 | 기준대비 |
|---|---|---|
| 비트코인 | 96,348,000 | ▼1,161,000 |
| 비트코인캐시 | 659,500 | ▼6,500 |
| 이더리움 | 2,830,000 | ▼31,000 |
| 이더리움클래식 | 12,440 | ▼140 |
| 리플 | 1,990 | ▼14 |
| 퀀텀 | 1,309 | ▼19 |
| 암호화폐 | 현재가 | 기준대비 |
|---|---|---|
| 비트코인 | 96,294,000 | ▼1,205,000 |
| 이더리움 | 2,831,000 | ▼30,000 |
| 이더리움클래식 | 12,440 | ▼140 |
| 메탈 | 409 | ▼10 |
| 리스크 | 185 | ▼1 |
| 리플 | 1,989 | ▼15 |
| 에이다 | 405 | ▼4 |
| 스팀 | 96 | ▲2 |
| 암호화폐 | 현재가 | 기준대비 |
|---|---|---|
| 비트코인 | 96,310,000 | ▼1,160,000 |
| 비트코인캐시 | 658,000 | ▼7,000 |
| 이더리움 | 2,836,000 | ▼25,000 |
| 이더리움클래식 | 12,450 | ▼180 |
| 리플 | 1,991 | ▼14 |
| 퀀텀 | 1,309 | ▲9 |
| 이오타 | 100 | ▲5 |