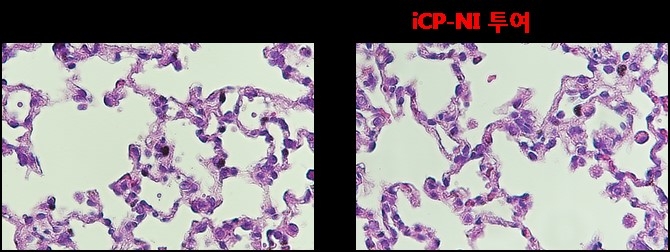
[로이슈 편도욱 기자] ㈜셀리버리가 코로나19 치료제로 개발중인 「내재면역 제어 항바이러스/항염증 면역치료제 iCP-NI」의 안전성 평가시험결과의 중간보고서를 수령하였다고 밝혔다. 사람에게 투여하는 효력농도 이상의 고농도를 소동물 (랫드)에 반복투여 하였는데, 조직병리 분석결과 어떠한 독성의 증거도 발견되지 않았다는 것이 핵심 내용이다.
해당 독성평가는 세계적으로 공인된 전문시험위탁기관 (CRO)인 미국 코방스 (Covance, 서머셋, 뉴저지주) 에서 진행한 것으로, 지난 5월 계약 이후 첫 중간결과를 보고한 것이다. 독성시험을 주관한 코방스 측 시험책임자 (Study Director) 미셸 트로이 박사 (Michelle Troy, Ph.D)는 “저농도 부터 고농도의 iCP-NI를 단계별로 소동물 100여 마리에 반복 투여한 결과, 효력농도 이상의 고농도에서도 사망 등 중대 이상반응은 물론, 조직병리상 그 어떤 이상소견도 관찰되지 않았으며 내부 장기의 이상반응을 보이는 개체도 없었다” 라고 보고 하였다고 회사측은 밝혔다.
일반독성시험 (general toxicity test)과 동시에, 안전성평가 중 중요한 분야인 유전독성시험 (micronucleus test) 시험책임자인 테레사 카이롬 박사 (Teresa Chirom, Ph.D) 역시, “권장 최고농도의 iCP-NI를 투여했음에도 DNA 손상이나 유전자 돌연변이, 염색체 이상, 세포분열기관의 손상이 발견되지 않았으며, 또 다른 유전독성시험 (AMES test)을 통해서도, 돌연변이체가 전혀 발생하지 않았다” 라고 보고 하였다고 회사측은 설명했다.
이러한 안전성 평가결과는 셀리버리의 내부 안전성시험에서도 재현되었다. 셀리버리측 연구관계자는 “현재 미국 써던리서치社 (Southern Research, 버밍햄, 알라바마주) 에서 수행중인 코로나19 영장류 치료효능 평가시험을 위해선 시험 시작 전에 반드시 무독성을 증명하여야 동물실험윤리위원회 (IACUC)의 승인을 받을 수 있었다.
이 효능평가시험 시작을 위해 써던리서치 측에서 요구한 모든 항목의 독성관련 실험을 이미 셀리버리 신약개발 연구소에서 실시한 바 있다. 시험결과, 효력농도 이상의 고농도의 iCP-NI를 소동물에 매일 투여 하였음에도, 그 어떤 이상소견이 발견되지 않았고, 내부 장기 조직검사 (histology) 에서도 염증, 세포사멸 (apoptosis)등 독성의 증거가 발견되지 않았으며, 17개 항목을 측정하는 혈액검사 (complete blood count: CBC test) 및 22개 항목을 측정하는 생화학검사 (blood biochemistry) 에서도 모든 항목이 정상수치를 나타냈다.” 라고 설명하였다.
셀리버리는 코로나19 바이러스 감염 영장류 효능평가시험 결과로, 산소 포화도 및 분당 호흡률 등의 임상증상 정상化와 폐 기관지 내 바이러스 수 감소효능 (대조군 평균 324%, 최대 540% 증가, 투약군 평균 84%, 최대 99.8% 감소)을 발표한 지 수 일 만에, 신약 개발과정 중 중요한 단계인 외부 전문시험기관이 수행한 안전성 평가시험을 통해 iCP-NI의 무독성을 입증하였다. 코방스는 현재 미국 FDA의 임상승인에 요구되는 GLP (good practice laboratory) 수준의 소동물 대상으로 2단계 시험 (200여 마리)인 장기 안전성시험과 대동물인 영장류 (원숭이 50마리) 대상 안전성시험을 계속해서 진행 중이다. 코로나19 사태를 종식시킬 치료제 개발을 위해, 평균 1년 6개월이 걸리는 안전성 평가시험 기간을 그 1/3 기간만에 종료하겠다는 계획으로 시험을 진행하고 있다고 회사측은 밝혔다.
㈜셀리버리 조대웅 대표는 “독성은 시험결과를 받아보기 전엔 그 누구도 장담하지 못하는 것인데, 이번 코방스의 소동물 독성시험 결과 무독성으로 분석되어 매우 다행이고 기쁘다. 또한, 인간과 매우 유사한 대동물 영장류 시험 결과가 곧 나올 것 이지만 마음은 가볍다.” 라고 소회를 밝히며, “조속히 모든 안전성 및 치료효능 평가시험을 완료하여 올 4분기 내 코로나19에 대한 구제약물 (salvage)로 미국 FDA 승인하에 임상시험 진입 하겠다. 또한, 동시에 치료목적사용승인 (expanded access programs: EAPs) 제도를 통해 미국에서 대단위의 코로나19 환자들에게 투여할 수 있도록, 법 규정을 지키면서도 빠른 진행을 위해 최선을 다하고 있다.” 라고 설명했다.
편도욱 로이슈 기자 toy1000@hanmail.net
셀리버리, 내재면역 제어 코로나19 면역치료제 iCP-NI 독성시험에서 안전성 입증
기사입력:2020-08-28 10:02:19
<저작권자 © 로이슈, 무단 전재 및 재배포 금지>
로이슈가 제공하는 콘텐츠에 대해 독자는 친근하게 접근할 권리와 정정ㆍ반론ㆍ추후 보도를 청구 할 권리가 있습니다.
메일:law@lawissue.co.kr / 전화번호:02-6925-0217
메일:law@lawissue.co.kr / 전화번호:02-6925-0217
주요뉴스
핫포커스
투데이 이슈
투데이 판결 〉
베스트클릭 〉
주식시황 〉
| 항목 | 현재가 | 전일대비 |
|---|---|---|
| 코스피 | 6,244.13 | ▼63.14 |
| 코스닥 | 1,192.78 | ▲4.63 |
| 코스피200 | 933.34 | ▼10.68 |
가상화폐 시세 〉
| 암호화폐 | 현재가 | 기준대비 |
|---|---|---|
| 비트코인 | 95,960,000 | ▲634,000 |
| 비트코인캐시 | 644,500 | ▲7,000 |
| 이더리움 | 2,830,000 | ▲24,000 |
| 이더리움클래식 | 12,390 | ▲100 |
| 리플 | 1,973 | ▲13 |
| 퀀텀 | 1,302 | ▲5 |
| 암호화폐 | 현재가 | 기준대비 |
|---|---|---|
| 비트코인 | 95,948,000 | ▲528,000 |
| 이더리움 | 2,831,000 | ▲19,000 |
| 이더리움클래식 | 12,360 | ▲50 |
| 메탈 | 399 | ▲3 |
| 리스크 | 181 | 0 |
| 리플 | 1,975 | ▲12 |
| 에이다 | 399 | ▲2 |
| 스팀 | 95 | ▲5 |
| 암호화폐 | 현재가 | 기준대비 |
|---|---|---|
| 비트코인 | 96,010,000 | ▲650,000 |
| 비트코인캐시 | 645,000 | ▲6,500 |
| 이더리움 | 2,828,000 | ▲21,000 |
| 이더리움클래식 | 12,360 | ▲60 |
| 리플 | 1,973 | ▲12 |
| 퀀텀 | 1,298 | ▼3 |
| 이오타 | 97 | 0 |